


خبرآنلاین/ یک مطالعه جدید نشان میدهد که همه سلولها با پیر شدن دچار تراکم پروتئین میشوند، درست مانند آنچه در اطراف نورونها در آلزایمر، پارکینسون و دیگر بیماریهای مغزی اتفاق میافتد. فهمیدن عملکرد آنها ممکن است راهبردهای جدیدی برای درمان بیماریهای مرتبط با افزایش سن را آشکار سازد.
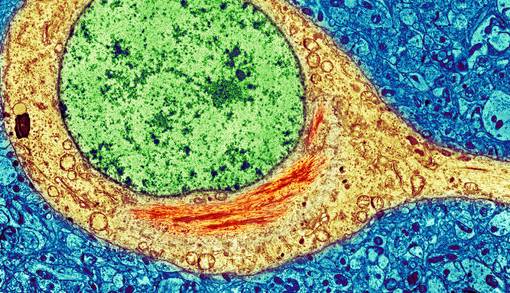
در تصویری که از نورون مغز یک بیمار مبتلا به آلزایمر گرفته شده، تجمعات غیر عادی پروتئین «تاو» به صورت کلافهایی از الیاف در نزدیکی هسته سلول ظاهر میشوند. چنین تجمعهایی از علائم بیماری هستند، اما به نظر میرسد که تجمع پروتئین با افزایش سن در سرتاسر بدن اتفاق میافتد.
مغز سالخورده و پیر افراد مبتلا به آلزایمر، پارکینسون و دیگر بیماریهای تخریب کننده عصبی، مملو از تودههای مشخصی از پروتئین در داخل و یا اطراف نورونها است. اینکه این تودههای پروتئین چطور ممکن است به نورونها آسیب بزنند، هنوز مشخص نیست، اما وجود این تودههای پروتئینی نشانه بارزی از این شرایط هستند.
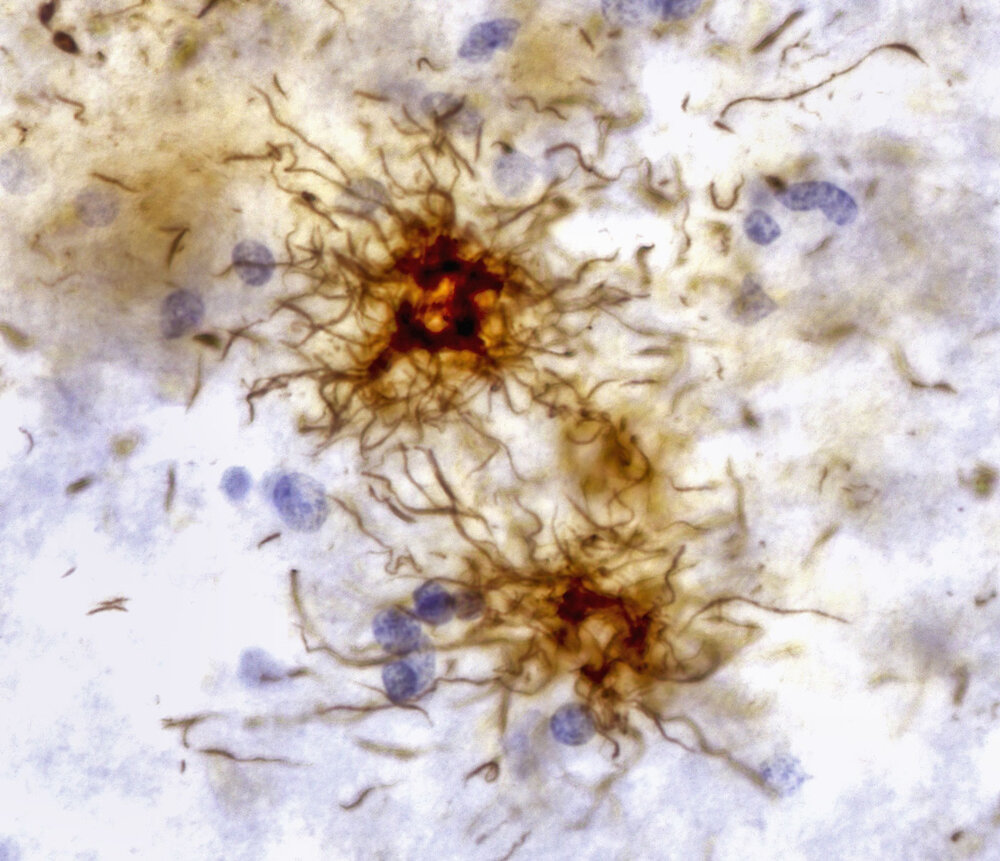
مطالعهای که اخیرا توسط تیمی از محققان دانشگاه استنفورد انجام شده نشان میدهد که تجمع پروتئین ممکن است یک پدیده کلی در سلولهای پیرشده باشند و میتواند نقش بیشتری نسبت به آنچه تصور میشد در بسیاری از بیماریهای پیری داشته باشند. این کشف ما را به سمت شیوه جدیدی از تفکر در مورد مشکلاتی که در سلول ها با افزایش سن رخ می دهد میبرد.
این تحقیق همچنین نشان میدهد که تجمع پروتئین با مکانیسمهای اساسی که به سلولها اجازه میدهد تا فیزیولوژی خود را با دقت و ظرافت بالایی تنظیم کنند، پیوند محکمی دارند. زیست شناسان باید با دقت و احتمالا با بررسی مورد به مورد، این موضوع را ارزیابی کرده تا بفهمند آیا تودههای پروتئینی برای سلولها تهدید محسوب میشوند یا از آنها دفاع میکنند.
در این مطالعه یک نوع ماهی که عمر آن بسیار کوتاه است مورد بررسی قرار گرفت. این پژوهش نشان داد که احتمالا تجمع پروتئین در طول زمان باعث زوال تدریجی بسیاری از بافتها میشود. همچنین این یافتهها اشاره به این دارند که چرا این تجمعات در مغز آشکارتر از سایر بافتهای بدن هستند: شاید علت آن این باشد که مغز به سرعت تکامل یافته است.
ماهی کیلیفیش فیروزهای آفریقایی(Killifish) در دریاچههای فصلی شرق آفریقا، که در فصول بارندگی شکل میگیرند، زندگی میکند. این ماهی زمانی که به پایان عمر کوتاه خود که بین ۴ تا ۶ ماه است نزدیک میشود، به تعدادی از بیماریهای مرتبط با افزایش سن از جمله آب مروارید و تغییراتی در مغز که شبیه اختلالات عصبی مانند آلزایمر در انسان است، مبتلا میشود. طول عمر کوتاه این ماهی، که حتی از موشهای آزمایشگاهی نیز کوتاهتر است، و سیر روند پیری طبیعی سریع، این ماهی را به مدلی ایدهآل برای مطالعه پیری در مهرهداران تبدیل کرده است.
داریو والنزانو، زیستشناس تکاملی میگوید: «نکته قابل توجه در مورد این ماهی این است که با افزایش سن، تنها تجمع پروتئین یا نارسایی قلبی یا اختلال عملکرد مغز رخ نمیدهد. بلکه در طول پیری تقریبا هر اندام و بافتی که به آن نگاه میکنیم، دچار تغییرات فاجعه باری میشود.»
تیم استنفورد تجزیه و تحلیل گستردهای در مورد پروتئینهای ماهی کیلیفیش در مراحل مختلف از جوانی تا بلوغ انجام دادند. در ماهیهای پیر با نگاه به تمام بافتهای سالخورده کشف کردند که در آنها تجمعات پروتئینی وجود داشت، این اندامها شامل نه تنها مغز، بلکه قلب، روده، کبد، عضلات، پوست و بیضه میشدند. در آزمایشهای بعدی بیش از نیمی از پروتئینهای انباشته شده تمایل ذاتی به متراکم شدن را نشان میدادند.
اما اینکه دقیقا کدام پروتئینها تجمع پیدا میکنند، از بافتی به بافت دیگر متفاوت است. بسیاری از پروتئینها اساسا در یک سطح در چندین بافت وجود داشتند، و در عین اینکه در یک بافت جمع میشوند در سایر بافتها اصلا انباشته نمیشوند.

شواهد خوبی از مطالعه بر روی کرم ها و مگس ها وجود دارد که نشان میدهد اگر سیستمی که ثبات و پایداری پروتئینها را حفظ میکند مختل شود، حیوانات سریعتر پیر میشوند. اگر مسیرهای کنترل کیفیت پروتئین از نظر ژنتیکی افزایش یابند، حیوانات عمر طولانیتری خواهند داشت. هیچ یک از اینها بیانگر این نیست که تراکم پروتئین باعث پیری میشود، اما بر این موضوع تاکید میکند که این دو ارتباط تنگاتنگی با هم دارند.
برای بررسی بیشتر رابطه بین تراکم پروتئین و پیری، محققان استنفورد، پروتئینهای موجود در انواع ماهی کیلیفیش که به طور غیرعادی سریع پیر میشوند را با دقت بیشتری بررسی کردند. این ماهیها در ژن آنزیم تلومراز خود دارای یک جهش هستند که طول کروموزومهای تقسیم شده را حفظ میکند. حیواناتی که دارای جهش تلومراز هستند معمولا به سرعت پیر میشوند.
جاروس گفت که او و همکارانش انتظار داشتند که در روده و سایر بافتهایی که به سرعت رشد میکنند و جایگزین میشوند، تراکم کمتری وجود داشته است: تقسیم سلولی اضافی به بافتهایی که به سرعت در حال رشد هستند فرصت بیشتری برای پاکسازی تودهها و بازسازی خودشان میدهد. اما عکس این مطلب اتفاق افتاد: بافتهایی که به سرعت رشد می کردند، پروتئینهای متراکمتری داشتند و نسبت به بافتهایی که آهسته رشد می کردند، سریعتر پیر میشدند.
بنابراین دوباره مشکلات مربوط به کنترل سلول بر کیفیت پروتئینهایش ممکن است توضیح این مطلب باشد. اگر سلولها کنترل خود بر فرآیندهایی که کیفیت پروتئینهایشان را حفظ میکنند از دست بدهند، با هر تقسیم سلولی آسیب بیشتری از تراکمها ایجاد خواهد شد. بافتهایی که به سرعت رشد میکنند، چون شانسشان برای متراکم کردن آسیب بیشتر میشود، سریعتر پیر میشوند.
علت اینکه چرا گاهی پروتئینها تجمع پیدا میکنند، پیچیده است. در کمال تعجب، بخشی از پاسخ این سوال به طور اساسی به یک مکانیسم ضروری به نام تراکم مرتبط است که سلولها برای کنترل پروتئینهای خود از آنها استفاده میکنند.
این که دقیقا چه چیزی باعث جذب پروتئینها و ایجاد تودهها میشود و این تودهها چقدر برای سلولها مشکل ایجاد میکنند، هنوز یک بحث بزرگ و خارقالعاده در این زمینه است. نمونه بسیار خوب از اثر محافظتی که از این مطالعات بدست آمده، پروتئین هانگتینتین است که برای رشد سالم سیستم عصبی ضروری است، اما در افراد مبتلا به بیماری هانگتینتون، یک جهش باعث شده تا پروتئین هانگتینتین به طور غیرطبیعی طولانی و بلند شود. سپس این پروتئین بلند به بخشهای کوچک و سمی تقسیم میشوند که به سیستم عصبی آسیب میزند.
در سال ۲۰۰۴، استیو فینکبینر، محققی که در زمینه پیری در موسسه گلادستون و دانشگاه کالیفرنیا، سن فرانسیسکو بر روی تجمع پروتئین هانتینگتین که در سلولهای عصبی کشت شده بود مطالعه ای را انجام داد. تیم او در این تحقیق نشان دادند که اگرچه تمام نورونهایی که دارای پروتئینهای غیرطبیعی هانتینگتین بودند، با گذشت زمان مردند، اما نورونهایی که در آنها تجمع هانتینگتین وجود داشت توانستند نسبت به نورونهایی که این پروتئین را نداشتند، زمان بیشتری را زنده بمانند.
از آن زمان او و دیگران نشان دادهاند که واکنشهای تجمعی حمایتی، در سایر بیماریهای نورودژنراتیو نیز اتفاق میافتد. این میتواند علت شکستهای پیدر پی آزمایشهای تجربی آلزایمر با هدف قرار دادن پلاکها را توضیح دهد. او در این باره میگوید: اگر پلاکهای آمیلوئیدی که معرف این بیماری هستند مانند پروتئینهای محافظتی به هم متصل شوند، شکستن این پلاکها ممکن است بیشتر از آنکه فایده داشته باشد، مضر باشد.
فینکبینر نوشت: «درک این مفهوم برای انسان دشوار است، زیرا این مطالب شهودی به نظر میرسند، و مفاهیمی که غیر عادی به نظر برسند باید «بد» و «بیماریزا» باشند. اما زیست شناسی علم پیچیدهای است که سرشار از عجایب است. بنابراین بسیار مهم است که مردم در نتیجهگیری فریب نخورند.»
نتیجه واضحی که اکنون به آن رسیده ایم این است که تجمع پروتئین پدیدهای مختص به بیماریهای عصبی نیست: این عمل بخشی از هر سلول است که به اندازه کافی عمر کرده و پیر شده است. بسیاری از پروتئینهای طبیعی و مهم مانند DDX5 تمایل به تجمع دارند، و مقابله با این تجمع یک چالش فراگیر است که هر سلول باید به آن رسیدگی کند.
از آنجایی که سلولها برای مدتهای طولانی با این مشکل دست و پنجه نرم کردهاند، پیشگیری از تجمع آنها ممکن است کاری مهم در تکامل توالیهای پروتئین باشد. از آنجایی که تعداد زیادی از پروتئینها آمادگی تجمع کردن را دارند، و جهشها این تمایل را افزایش میدهند، به احتمال بسیار قوی، تعداد زیادی از پروتئینها، به طور طبیعی در مقابل جهش ایستادگی میکنند. (این نتیجه گیری در نتیجه این موضوع است که در حیوانات جوان، بیشتر پروتئینها تمایل کمی به جهش دارند). بنابراین پروتئینهایی که تعداد آنها کمتر است ممکن است سریعتر از آنهایی که تعدادشان زیاد است تکامل پیدا کنند و نرخ تکامل آنها باید با تمایلشان به تجمع همخوانی داشته باشد.
این اثر در مغز ماهی کیلیفیش بسیار بارز بود. محققان بر این گمان هستند که این پروتئینها ممکن است کلید نوآوری در اندام بوده باشند. اگر چنین باشد، تغییرات تکامل در مغز که آن را به عضوی مهم در مهرهداران تبدیل کرده است، میتواند این عضو را در برابر بیماریهای تخریبی ناشی از تجمع آسیبپذیرتر کرده باشد.
در واقع این احتمال وجود دارد که هر بافت و اندامی باید به تعادلی متفاوت برای انجام کارهای خود و مدیریت تجمع پروتئین برسد. هر بافتی نیازها و محدودیتهای عملکردی منحصر بفرد خود را دارد: سلولهای روده دائما در حال تغییر هستند؛ سلولهای غدد درونریز هورمون ترشح میکنند؛ سلولهای مسئول ایمنی بدن زمانی که مهاجمی را شناسایی میکنند وارد عمل میشوند؛ مغز اطلاعات را پردازش میکند. کارهای مختلف نیاز به پروتئینهای متفاوت دارند و این یعنی استراتژی تکامل یافته برای مقابله با تجمع پروتئین از بافتی به بافت دیگر و از حیوانی به حیوان دیگر متفاوت است. میتوان گفت از آنجایی که مغز مهره داران در گذشته نه چندان دور بسیار سریعتر و گستردهتر از مثلا عضلات آنها تکامل یافته است، ممکن است دستگاه کنترل کیفیت پروتئین آن هنوز زمان کافی برای تکامل سیستم محافظتی کافی در برابر تجمعهای پروتئینی نسبتا جدید را نداشته باشد.
با این وجود مشکل اساسی تجمع پروتئین برای همه موجودات وجود دارد، و این مشکل فقط منحصر به زمانهای بیماری یا استرس شدید نیست و این یک واقعیت است که تجمع پروتئین در سرتاسر بدن عاملی برای پیری در موجودات مختلفی مانند مخمرها، کرمها، مگسها، ماهیها، موشها و انسان است.